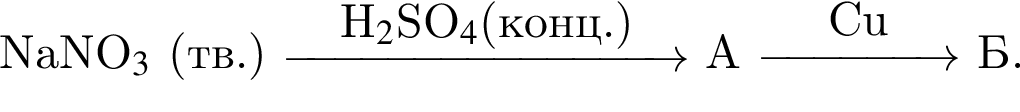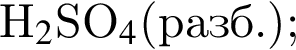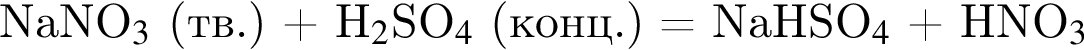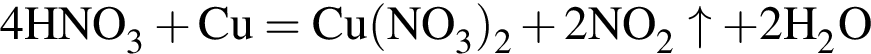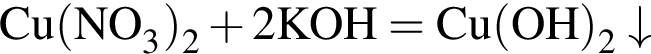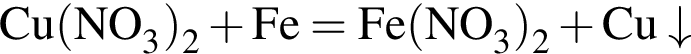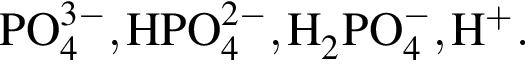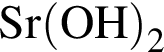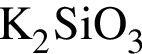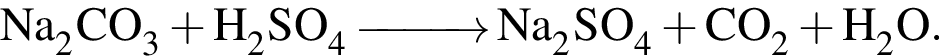В четырех пронумерованных пробирках находятся разбавленные растворы неорганических веществ. О них известно следующее:
- растворы из пробирок 2 и 3 нейтрализуют друг друга;
- при добавлении хлора в пробирку 1 образуется красно-коричневая жидкость (н. у.);
- при смешивании содержимого пробирок 2 и 4 выпадает осадок, который растворяется как в кислотах, так и в щелочах.
Установите соответствие между названием вещества и номером пробирки, в котором находится раствор данного вещества.

Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например, А1Б4В3Г2.
![]() ;
;![]() ;
;
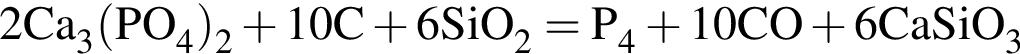
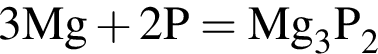 ;
; 
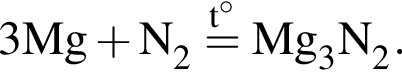 Так степень окисления азота в процессе реакции изменяется от 0 до -3, то он выступает в роли окислителя;
Так степень окисления азота в процессе реакции изменяется от 0 до -3, то он выступает в роли окислителя;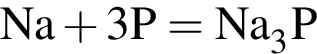
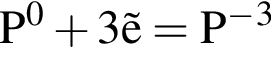 - окислитель
- окислитель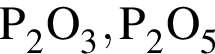 .
.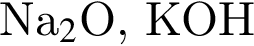
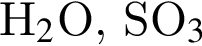
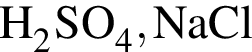
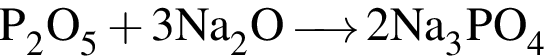 .
.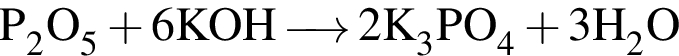 .
.
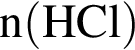 = 73,5/81=0,907 моль
= 73,5/81=0,907 моль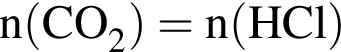 =0,907 моль
=0,907 моль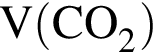 =0,907 · 22.4=20,3
=0,907 · 22.4=20,3
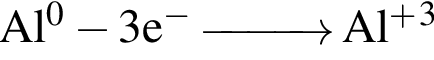
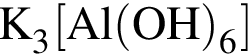 )=1066 г/246 г/моль=4,33 моль
)=1066 г/246 г/моль=4,33 моль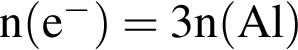 =13 моль
=13 моль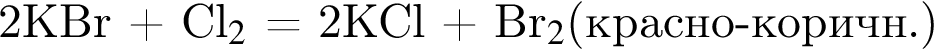 значит, в 1-й пробирке находится бромид калия.
значит, в 1-й пробирке находится бромид калия.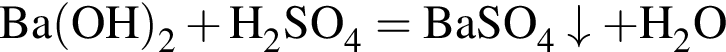 - реакция нейтрализации. Тогда в оставшейся 4-й пробирке находится нитрат цинка.
- реакция нейтрализации. Тогда в оставшейся 4-й пробирке находится нитрат цинка.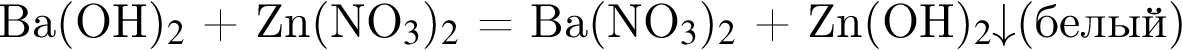
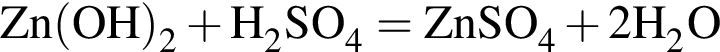
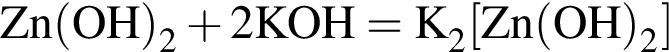
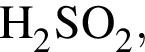 Broken TeX Broken TeX 80 г.
Broken TeX Broken TeX 80 г. 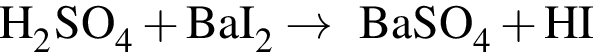
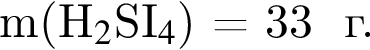
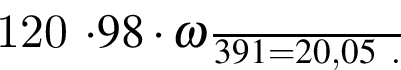
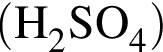
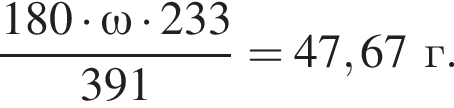
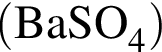
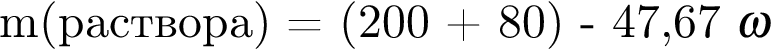
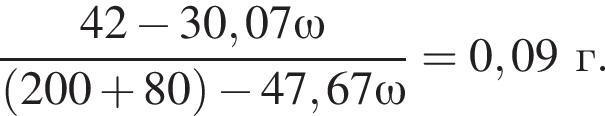
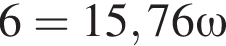

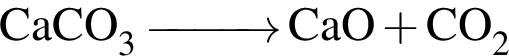
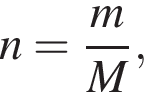 где n — число молей, m — масса вещества, M — молярная масса данного вещества, находим массу фосфора в 100 г аммофоса:
где n — число молей, m — масса вещества, M — молярная масса данного вещества, находим массу фосфора в 100 г аммофоса: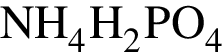 ) = 115x г.
) = 115x г.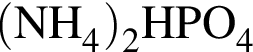 ) = 132y г.
) = 132y г.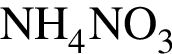 ) = (112 − 73) · 80/28 = 111 г.
) = (112 − 73) · 80/28 = 111 г.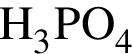
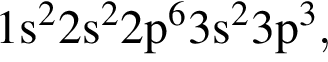 находится в группе:
находится в группе:
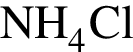
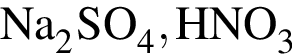
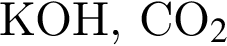
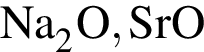
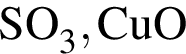
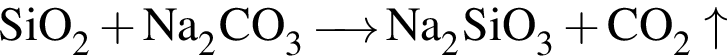 .
.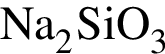 , В —
, В — 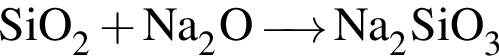
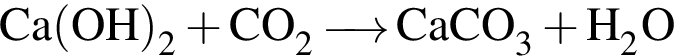 .
. 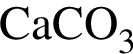
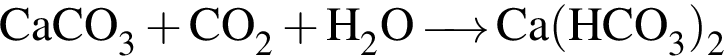 .
.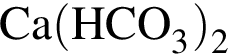
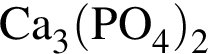 равна 310.
равна 310.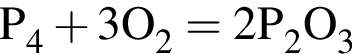
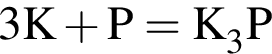
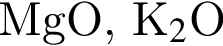
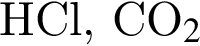
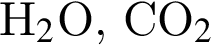
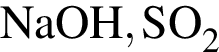
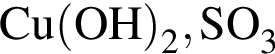
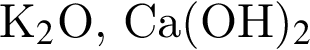
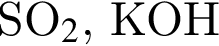
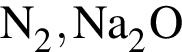
 . Количество молекул
. Количество молекул 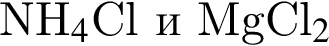
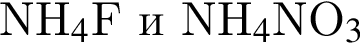
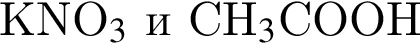
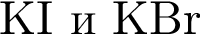
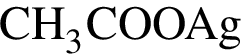
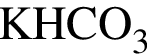
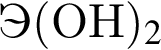 :
: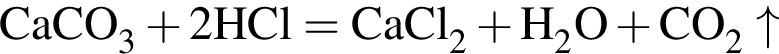
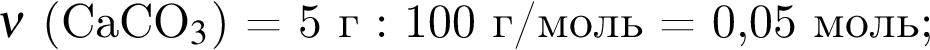
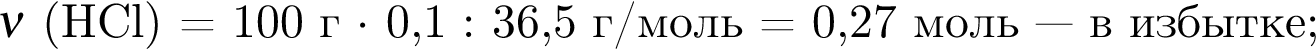
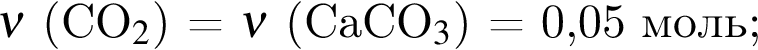
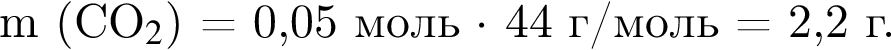
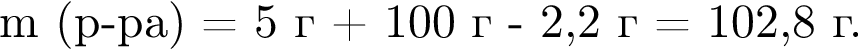
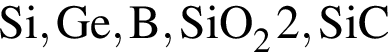 (карборунд),
(карборунд), 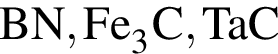 , красный и чёрный фосфор. В эту группу входят, как правило, твёрдые и тугоплавкие вещества.
, красный и чёрный фосфор. В эту группу входят, как правило, твёрдые и тугоплавкие вещества.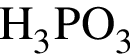
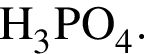 Массовая доля кислорода составляет:
Массовая доля кислорода составляет: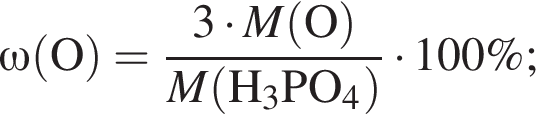
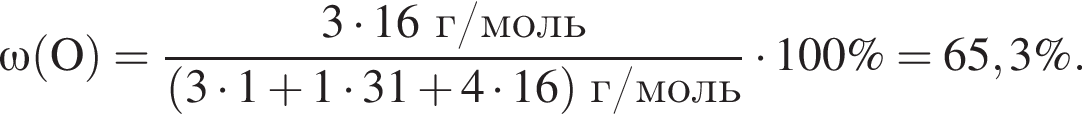
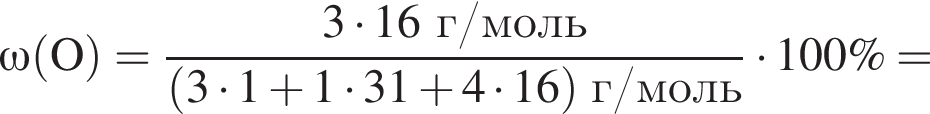
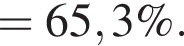

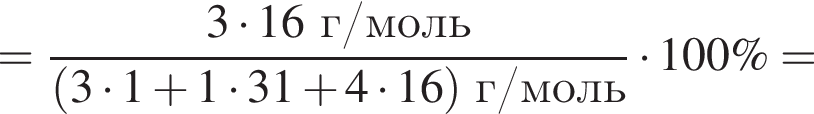

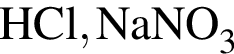
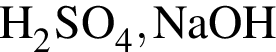
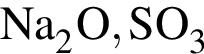
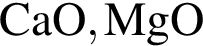
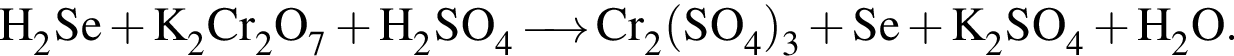
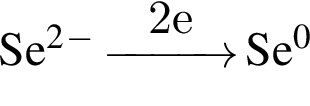
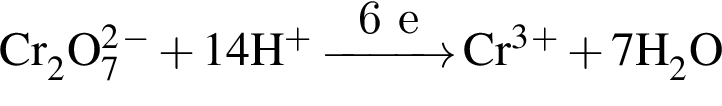
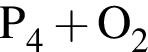 →
→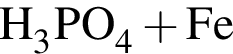 →
→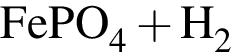
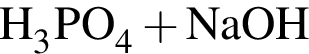 →
→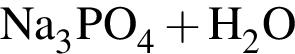
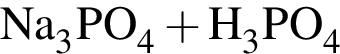 →
→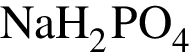 М=120
М=120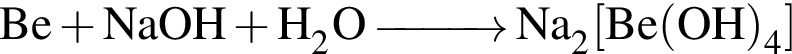



 . Запишем уравнение реакции сгорания алкина:
. Запишем уравнение реакции сгорания алкина: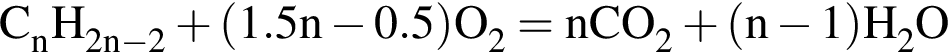
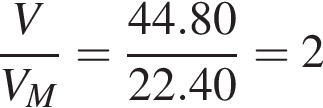
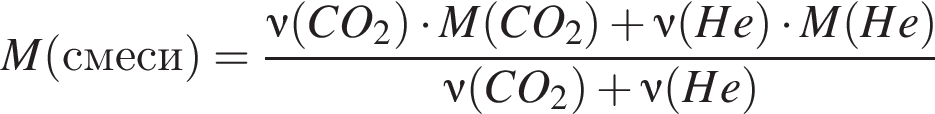
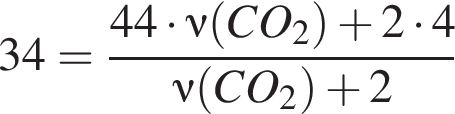
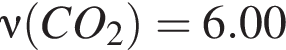 моль
моль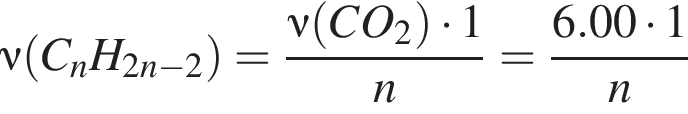
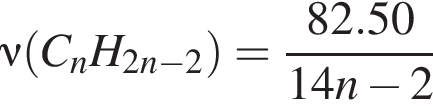
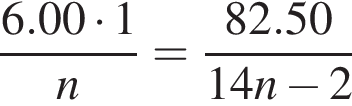
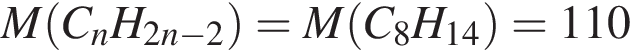 г/моль
г/моль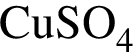 и 1 моль
и 1 моль 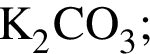

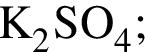
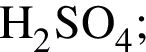
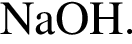
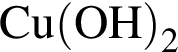 количеством 0,5 моль:
количеством 0,5 моль: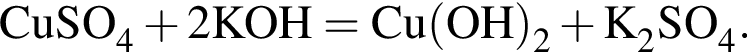
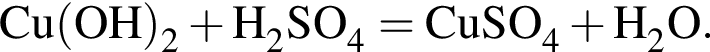
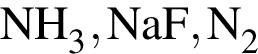
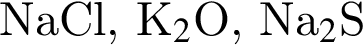
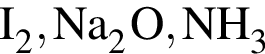
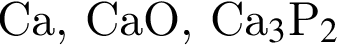
 наблюдается:
наблюдается: